
 |
|||
智能流体处理产品带您走得更远更快
Smart fluid handling to take you forward,faster |
|||

|
工艺放大:搭建真正的封闭系统以实现CGT产品规模化生产
毫无疑问,生物制药的下一个热点来自再生医学。从ARM 2020的一份统计数据来看,去年全球有超过1,085家从事再生医学的公司,其中美国以543家位居全球首位。中国也以近300家位列第二,超过了欧洲。 放眼全球的细胞与基因治疗(CGT)领域,每年大概有1,000个临床实验在进行,同时FDA每年会收到超过200个IND申请。根据Accenture对CGT市场的预测,到2030年,获批上市的CGT产品数量将会达到60个,比2025年的预测翻了3倍。 这就带来一个问题:我们如何能有效且主动地在短时间内将疗法安全快速地带给患者? 对于中小型CGT公司来说,高速增长的挑战在于目前的规模无法满足生产。数据预测可能会有超过65%的公司会考虑转向第三方技术服务公司外包。需求的叠加将把压力转移到那些原本小规模的CDMO/CRO公司。 这些因素都可能会直接导致产品无法如期投入市场。有些产品的研发计划可能会被推迟,终导致病患无法得到医治。在这次的新冠疫情中,从业者就对这个矛盾深有体会。 我认为,解决规模问题的方法在于工艺的优化和放大。
提升工艺放大的效率
我们可以通过一个常见的例子来理解工艺放大:在一开始,研究人员使用单通道移液枪,然后增加成8通道移液枪,后扩大到12通道的电子移液枪。 这个过程是开放的,而且以人员操作为主,需要通过环境控制来确保无菌条件。当进入小试阶段,我们开始用可以放大的封闭系统来代替96孔板,比如小型的细胞工厂或反应器。在细胞培养的过程中,还需要额外控制pH和溶氧等关键因素。 这就是工艺放大的过程——从实验室级别到反应器,然后再一步步增加反应器的体积。 例子中开放系统的劣势在于,每一个步骤都需要依赖操作人员的经验,整个过程的不可控性较高,对操作人员的要求也更高,每次的结果都有可能受到人为影响。 这些挑战大大阻碍了工艺放大的效率。特别是在中试和生产阶段,开放系统的劣势就更加明显。

当然,无菌操作也是一个问题。小规模的系统可以通过层流罩或超净台来实现局部无菌环境。但随着一次性技术的发展,一些制药公司逐步开始将关键步骤用封闭系统代替,从开放系统转变为半封闭系统。
半封闭系统虽然在一定程度上优化了工艺流程,但有些需要无菌操作的部分仍然依赖层流罩之类的设备来控制环境。半封闭系统也无法通过自动化控制系统对整个工艺参数进行记录和控制。
我们总结了CGT企业在工艺放大的过程中可能会遇到的几个挑战: 1,缺少相对一致的工艺流程,放大线性系数差,更多的是依赖人工操作。这也对日后整个生产上自控系统带来了阻碍。 2,企业对于时间节点的把握缺乏经验,但是又承受着成本以及产品上市的压力。由于CGT是一个新兴的领域,很多时候企业在摸着石头过河,对于工艺的推进也会比较保守,前期不太愿意花太多的投资在工艺优化和升级上。 3,缺少熟练的操作人员。不仅是CGT,整个生物制药行业因为市场增长太快,都缺少专业人员。在职人员必须超负荷工作,长期以往会影响工作效率。这个人才缺口还将随着下一个热点的来临持续加大。 4,当自身产能不足时,我们会想到找CDMO/CRO合作,但是这本身也是一个挑战。找谁合作更合适?CDMO目前自身的产能也在接近饱和,如果扩产则需要新建厂房,这将花费更多的时间和投资成本。
封闭系统:工艺放大的佳方案
上述的这些挑战可以通过封闭系统来应对。 第一,基于一次性技术(SUT)的封闭系统可以实现独立的、类似洁净室的保障。 众所周知,改造一个洁净室的成本非常高昂,尤其是A级洁净室。这也是为什么很多企业会考虑通过层流罩来实现局部无菌环境。但是如果使用封闭系统,多余的花费就不存在了。基于SUT的封闭系统对操作环境没有任何要求,哪怕在GMP C级环境下也可以实现无菌操作。由于是一次性使用,系统无需清洗验证,没有交叉污染,降低风险。生产工艺中的操作人员的安全也能被更好地保护,使工作场地更符合EHS要求。
实现真正的封闭系统 我认为,当所有的耗材均为预组装,才能实现真正的封闭系统。
以两种常见的工序连接方式作为比较:
热塑管+焊管机:
- 需要自行操作焊接过程。 - 焊接时候需要用刀片切割,高温会导致软管断裂,可能会发生溶出物和颗粒物污染。 - 热塑管仅限于管径一致的同管材,甚至限于同品牌同型号之间才能够热焊连接。 - 需要额外的焊管机设备。
无菌连接器:
- 连接步骤简化至少3步就能完成,过程仅需几秒,操作风险极低。
- 可以在在非无菌环境下实现无菌对接。 - 连接部位是无菌接头而非管路,因此对管材管径均没有要求,可以在任意的管材间连接与变径。 - 在常温环境下操作,不影响管路本身。 - 不需要额外的设备加固。 由此可见,无菌连接器作为一种SUT,可以在系统关键的连接处大幅减少操作风险、简化操作流程,避免系统暴露并受到污染侵害,真正做到全“封闭”。

上游细胞培养 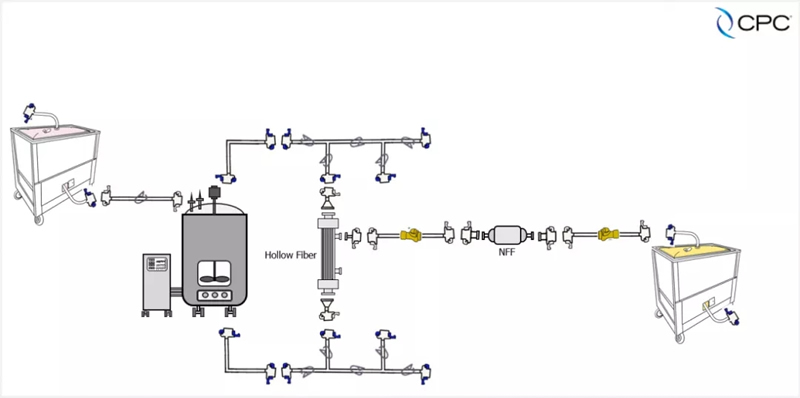
下游纯化过滤
无菌连接的其它主要优势包括: - 连接器经过完整验证,内容包括可提取物验证、无菌验证、低温冻存验证、压力测试、爆破测试、蠕变测试、负载测试等,有助于降低生物企业的验证成本。 - 从有性别到无性别的不分公母无菌连接器,可以说是一个里程碑式的变革。对采购来说,物料管理成本降低一半;对操作人员来说,无性别在使用时出错率也更低。
CGT工艺中需要使用到SUT的情景有很多。比如自体工序和病毒载体的生产,每一步连接都需要合适的技术以确保其安全和高效。又比如在病毒载体生产过程中,从载体放大和种子培育到生物反应器中的载体扩增,再到澄清和纯化,后进行过滤和灌装,将其倒入成品容器中,每一步操作都需要连接技术的支持。
即使在一种部件类型中(如储液袋、接头或细胞培养系统)中,SUT 的数量都是惊人的。因此,新用户会经历一个陡峭的学习曲线。我们鼓励CGT企业向专业的流体处理专家详细了解适合您应用的 SUT知识。
 参考资料 [1] ARM 2020 State of the Industry Report [2] Srivastava S. How Cell And Gene Therapy Is Transforming Healthcare, Cell & Gene, Feb. 2020
CPC成立于1978年,是生物制药、细胞和基因治疗市场的一次性连接器技术的领先设计和制造商。CPC专注于研发针对生物和再生医学市场的接头产品,在生物制药领域有超过20年的经验。考虑到行业的飞速发展和客户不断增长的需求,CPC今年继续扩容仓库,增加安全库存。
|
||||||||||||||||||
We inspire confidence at every point of connection.
京公网安备11010502019739 |
陕ICP备11000581号-1
| 联系我们 |
|
 加我微信 |
 公众号 |
|||||||||||||||
|
||||||||||||||||||